随着全球新型冠状病毒肺炎疫情风险升级,口罩等防疫物资一度出现告急,就连世界卫生组织都表示:新型冠状病毒肺炎疫情已经导致目前对口罩、手套的需求量是正常水平的100倍,个人防护用品的长期短缺将成为人类应对这场肺炎疫情的巨大挑战。
最近很多人都来电咨询口罩出口是否被限制问题,口罩出口没有限制,但要注意进口国的要求以防到达国外后资质不符合而无法清关,东浩物流小伙伴搜集了关于口罩出口欧洲美国进口的法规要求详解资料,分享给大家
在此情况下,口罩商机很快将转移到国外,那么口罩在欧洲、美国的分类、准入门槛及有什么要求? 东浩物流搜集整理了口罩出口欧洲美国进口的法规要求详解如下:
口罩按其预期用途,可以分为个人防护口罩和医用口罩两大类别,在欧美依据不同的法规在管理。
个人防护口罩
欧洲PPE
个人防护口罩的欧洲标准是EN149,按照标准将口罩分为FFP1/FFP2和FFP3三个类别,具体的指标如下:

欧洲防护口罩分类
认证的申请:
企业需选择有PPE法规授权的公告机构(Notified body)实施申请,NB机构需审核企业质量管理体系和CE技术文档。审核通过后可获得PPE法规的CE证书。
美国NIOSH
根据联邦法规42 CFR Part 84,NIOSH将其认证的防颗粒物口罩分成N95、N99、N100、R95、R99、R100、P95、P99、P100合计9个类别。具体的测试则由NIOSH下属的NPPTL (National Personal Protective Technology Laboratory)实验室操作。
从某种意义上来说,N95算是其中防护级别比较低的品类。
上述9种口罩需满足美国联邦法规42 CFR Part 84的要求,主要测试指标包括唿气阻力测试(Exhalation Resistance Test)、唿气阀泄漏测试(Exhalation Valve Leakage Test)、吸气阻力测试(Inhalation Resistance Test)、过滤效率测试(Sodium Chloride Test)。
认证的申请:
需按照NIOSH的指南实施,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系部分资料)至NIOSH文审,只有文审和测试都通过,NIOSH才核发批文。
医用口罩
欧洲CE
医用口罩对应的欧洲标准是EN14683,该标准对于口罩的分类如下图所示,按照BFE、唿吸阻抗和防喷溅能力分为三个类别,如图所示:
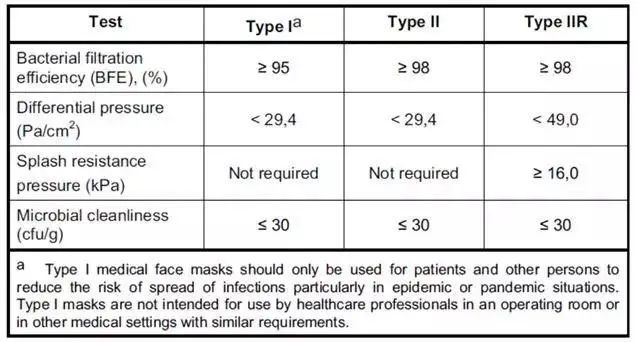
欧洲医用外科口罩的分类
按照医疗器械法规2017/745/EU的要求,口罩产品可以按照一类器械进行管理。依据产品是无菌或非无菌状态提供,其认证模式不一样。
美国进口口罩要求:
美国FDA
美国对于医用口罩的管理机构是FDA,在FDA系统中对于口罩的分类代码有如下3个。其中一个是外科口罩,一个是儿科口罩,一个是带有抗菌/抗病毒介质的外科口罩,如图所示。

美国FDA分类数据库中的口罩
三个类别的口罩都属于规则878.4040,分类都是II类,都需要申请510K批准。那么我们正常出口美国的口罩必须的路径为:
1.进行产品测试(性能测试、生物学测试)
2.准备510K文件,提交FDA评审
3. FDA发510K批准信
4. 完成工厂注册和器械列名
5. 产品出口
以上关于口罩出口到欧洲/美国的当地国家的进口要求,仅供参考,安全起见实际出货前请让收货人与当地海关确认进口要求和资质等信息,以免导致无法清关提货的损失。

